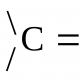온도가 다른 두 기체를 혼합합니다. Zmіshuvannya gazіv. 화학열역학의 기초
13.7. 열 변압기
대부분의 기술 프로세스는 동일한 온도를 유지하는 데 필요합니다.
이러한 종류의 냉각의 가장 간단한 방법은 불을 태우고 뜨거운 연소 생성물에서 열을 전달하거나 중간 열 또는 중간 열을 사용하지 않는 것입니다. 온도가 높은 뜨거운 dzherel 방향으로 자연 경로에 의해 어떤 열 교환이 수행됩니까? 티온도가 있는 감기 1회 티 2. 이 방법을 사용하면 불을 태울 때 따뜻함이 더 높고 otrimane이 낮아서 옮길 수 없습니다 (그리고 비용과의 연결이 훨씬 적습니다).
그러나 원칙적으로는 가능하며 많은 따뜻함이 어렴풋이 나타납니다. 큐" 고온용 티 1, 일을 사용하지 않고 더 낮은 온도에서 더 많은 열을 꺼내십시오. 티 2. 고온 매체와 고온 매체 사이에 역 직접 카르노 사이클을 생성하는 것으로 충분합니다. 티 시간, 그 결과 로봇으로 이동합니다(div. (7.7)):
Vitrativshi tsyu는 온도 T가 있는 매체 사이의 역방향 순환 Carnot에서 작동합니다. 시간온도와 진정 티 2, 건강한 온기를 남에게 전하자
이 맥락에서 로봇의 의미를 대체 엘 시간전면 virazu에서 다음을 수행합니다.

비례 계수 ψ 1.2라고합니다. 열 변환 계수온도에 따라 티 1 최대 온도 티 2 .
Otzhe, 오트리마브시 큐" 온도에 따른 dzherel의 열량 티 1 체온으로 신체에 전염될 수 있음 티 2 열량 ψ 1.2 큐" .
그래서 야크 티 2 T 1 다음 i 큐" >큐" .
예를 들어 티 1 = 1000 프로 Z, 티 2 = 50 프로 Z, 티 시간 C에 대해 = 0. 계수. 이와 같이, 예를 들어 약 50℃의 온도에서 5J의 열을 취하기 위해서는 약 1000℃에서 1J 미만의 열을 취해야 하는 반면, 원시 스코칭 설비의 경우에는 1J의 고온의 열은 저온의 열량으로 전달되어야 합니다.
또한 열역학을 한 눈에 볼 때 오팔 설치는 5배 덜 경제적이며 역방향 열 전달 설치가 더 낮습니다.
동일한 온도의 dzherel에서 더 낮은 온도로 열 전달의 직접 및 역방향 순환을 허용하는 부착물을 호출합니다. 열변압기.
주말 동안 온도를 낮추어야 하는 경우 열변압기를 호출합니다. 저하.
고온, 저풍을 낮추려면 추가 도움이 필요합니다. 이동하다일부에게는 열변압기, 그래서 야크 티 2 > 티 1 .
쌀. 13.7 소형 13.8
열기관 및 히트펌프용 열변압기.
무화과. 13.7은 강압 열 변압기의 다이어그램을 보여줍니다. 13.8 - 요고 이론적 순환.
무화과. 13.9는 움직이는 열변압기의 다이어그램을 보여줍니다. 13.10 - 요가 이론적 사이클.
그림에서 : І - 열 엔진, ІІ - 히트 펌프.
온도를 낮게 유지하기 위한 약속의 열변압기로서 더 높고 더 낮은 출력을 vin이라고 합니다. 혼합형 열변압기.
쌀. 13.9 작음. 13.10
영양 조절
Carnot의 역전주기는 어떻게 작동합니까?
열 펌프 설치의 열역학적 효율을 평가하는 매개변수는 무엇입니까?
히트 펌프 및 냉동 장치의 중요한 계획은 무엇입니까?
14. 가스와 증기의 변화
다양한 별채에서 어머니는 종종 다양한 가스, 증기 및 공기의 zmіshuvannyam에 의해 오른쪽으로 이동합니다. 이 경우 매개변수를 지정해야 합니다. I는 주어진 매개변수의 합계가 됩니다. I는 구성 요소가 되어 합계의 합계를 결정합니다.
이 작업의 성취는 이 변화 과정이 만들어지는 마음에 있습니다. 합계를 만드는 모든 방법은 세 그룹으로 나눌 수 있습니다.
일정한 obsyazі에서 zmіshuvannya gazіv,
가스 흐름의 혼합,
zmіshuvannya gazіv pіd 시간 zapovnennya 탱크.
14.1. 게시물을 변경하는 과정
바이스에서 가스를 뿌린다는 사실에 합계의 합계를 만드는 방법은 무엇입니까? 아르 자형 1 , 아르 자형 2 , …, 아르 자형 N, 온도 티 1 , 티 2 , …, 티 N타 마사미 G 1 , G 2 , …, G N다른 의무를 빌리다 V 1 , V 2 , …, V N(그림 14.1).
가스 사이에 퍼지는 칸막이를 정리하면 가스가 혼합되어 있습니다.
V = V 1 + V 2 + …+ V N ,
그리고 많은 미친
G = G 1 + G 2 + …+ G N .
똑같이 중요한 것을 설치하면 합계의 매개 변수는 아르 자형, V, 티, 유.
단열 프로세스가 변경되지 않으면 시스템의 내부 에너지가 열역학의 첫 번째 cob에 저장됩니다.
유 = 유 1 + 유 2 + …+ 유 N또는 구=지 1 유 1 + 지 2 유 2 + … + G N 유 N .
애완 동물의 내부 에너지는 다음과 같이 측정됩니다.
![]() , (14.1)
, (14.1)
드 g 나- 질량 분율 나가스.
그리고 애완 동물은 그의 약속에 동의했습니다
![]() . (14.2)
. (14.2)
기타 매개변수( 아르 자형, 티) 실제 가스의 경우 parіv 및 rіdin은 이러한 연설의 다이어그램에서 찾을 수 있습니다.
서늘한 분위기에서 열용량이 일정한 이상기체를 혼합하면 뒤= 씨 V dT, 찍은
 이 경우 동일한 가스의 일부가 변동하는 경우 더 간단한 공식을 사용하여 합계의 온도를 계산합니다.
이 경우 동일한 가스의 일부가 변동하는 경우 더 간단한 공식을 사용하여 합계의 온도를 계산합니다.
![]() .
.
변경 후 가스의 압력은 Klaiperon-Mendeliev와 동일하게 청구됩니다.
드 아르 자형- 가스는 스미시가 되었습니다(섹션 1.4에 지정됨).
14.2. 스트림을 혼합하는 과정
이러한 방식으로 가스의 변동은 하나의 채널에 많은 흐름이 축적된 결과로 발생합니다.
파이프라인을 보자 1 (그림 14.2) 매개변수가 있는 가스는 혼합 챔버에 공급되어야 합니다. 피 1 , V 1 , 티 1 , 시간 1, 파이프라인을 통해 2 – 매개 변수가 있는 가스 피 2 , V 2 , 티 2 , 시간 2 .
파이프라인을 통한 Vitrata 가스 1 dorivnyuє G 1, 파이프라인을 통해 2 – G 2. 챔버 입구에서 챔버를 누르기 위해 혼합 및 가스 흐름이 조절됩니다. 아르 자형더 적게, 더 낮게 아르 자형 1타 아르 자형 2(약비, 예를 들어, 아르 자형 > 아르 자형 1, 그러면 챔버의 가스가 파이프라인으로 돌진합니다. 1 ).
다음 목소리, 무슨 악덕 아르 자형챔버에서 환기를 다르게 조정할 수 있습니다(밸브 조정). 전류의 요동 과정은 정상 상태의 요동과 정확히 동일합니다.
매개변수와 가스를 혼합하는 챔버에서 아르 자형,V, 티관로 3 . 파이프라인의 Vitrata 가스 3 , 분명히, dorivnyuє G = G 1 + G 2 .
파이프 라인에 흩어져있는 가스가 무너지면 krіm vnutrishnyoї energії, vіn maє (yak tіle) sche 및 운동 및 위치 에너지. 단순함을 위해(더 많은 기술적 문제의 경우 사실임) 다음이 중요합니다.
수평 roztashovan 파이프라인, zm_noy 위치 에너지는 znehtuvat일 수 있습니다.
이동하는 가스의 속도는 작아야 합니다. 변화하는 운동 에너지도 넥투예모입니다.
단열 흐름(9.3)에 대한 첫 번째 코브와 동일합니다.
땀에 zmіshuvannya의 결과로 애완 동물 enthalpії sumіshi, otrimana에 대한 Zvіdsi otrimaєmo viraz :
![]() . (14.3)
. (14.3)
반려동물의 엔탈피 알기 시간그 바이스 아르 자형가스를 변경한 후 추가 다이어그램을 위해 합계의 다른 매개변수를 알 수 있습니다( 티, V, 에스그리고 안으로.).
이상기체의 경우 이 엔탈피를 viraz로 대체 시간 아르 자형 티, 찍은
![]() . (14.4)
. (14.4)
한 기체의 두 흐름을 혼합할 때 합의 온도 공식은 간단합니다.
![]() . (14.5)
. (14.5)
그런 순위에서 온도를 아는 것 티, 나는 이상 기체에 대해 동등해질 것입니다. 사소한 obsyag를 알 수 있습니다.
공식 (14.3)–(14.5)은 변동하는 특정 수의 가스 흐름에 대해 유사한 방식으로 작성됩니다.
14.3. 의무 당시의 기억
탱크로 이동 1 (그림 14.3) Vє 가스 (증기, 조국) G매개변수가 있는 1 아르 자형 1 , 티하나 . 탱크에 파이프라인이 있는 탱크 2 가스 іz 매개변수 아르 자형 2 , V 2 , 티 2 (분명히, 뭐 아르 자형 2 > 아르 자형 1) 질량 기준 G 2 그 후 밸브가 닫힙니다. 저수지에서 가스가 한가득 나온다 V그 마소유 G = G 1 + G 2. 취한 합계의 매개 변수를 지정해야 합니다.
충전 공정에서 파이프라인의 가스 위에 로봇이 설치되고 있습니다. 2 , 리브나 – 피 2 V 2 G 2; 저수지에는 로봇이 없으며 파편은 저수지에 고정되어 있습니다.
로봇의 단열 과정에서 균형을 위해 내부 에너지를 변경해야 합니다(이전과 같이 흐르는 가스의 운동 에너지, 흐름의 유동성 부족을 볼 수 없음).
선박의 Zvіdsi 애완 동물의 내부 에너지 sumish는 건강합니다.
![]()
Pitoma 돈을 위해 많은 금액 V = V/ G.
앎 유і V, 추가 다이어그램의 경우 다른 매개변수 sumishi( 아르 자형, 티, 에스, 시간).
열용량이 일정한 하나의 동일한 이상기체를 혼합할 때
드 케이- 단열 지표.
탱크의 바이스
두 부분이 일렬로 혼합되고 첫 번째 성분의 무게는 10kg이고 온도는 400°C이고 다른 성분의 질량은 90kg이고 온도는 100°C입니다.
솔루션: 영구 환기의 경우 변동 프로세스의 결과로 총 온도 또는 가스 흐름의 변동 프로세스는 공식에 따라 달라집니다. 티 = g 1 티 1 +g 2 티 2. 우리 응용 프로그램의 І가 더 비쌉니다. 티\u003d 0.1 ∙ 400 + 0.9 ∙ 100 \u003d 130 pro C.
첫 번째 가스가 이미 알려진 약속의 결과로 요약되면 절대 온도는 다음 공식에 따라 계산됩니다. 티 = g 1 티 1 +킬로그램 2 티 2. 이 엉덩이는 다시 adiabati 표시가 있습니다. 케이= 1.4 티\u003d 0.1 (400 +273) +1.4 ∙ 0.9 ∙ (100 +273)-273 \u003d 264 약 C.
14.4. 변경시 엔트로피 변경
sumish의 엔트로피는 창고 qiu sumish, tobto의 엔트로피의 합입니다.
그러나 애완 동물 크기
변화의 과정은 돌이킬 수 없는 과정이기 때문에 열역학 시스템의 엔트로피(단열적 언어 변화의 모든 것)는 그 과정에서 다른 열역학의 속과 유사합니다.
혼합 과정의 비가역성은 과정에 수반되는 혼합 성분의 확산으로 설명됩니다. 불가역의 세계에서 변화 과정에서 엔트로피의 증가.
영양 조절
혼합의 주요 방법은 무엇입니까?
sumish를 얻는 방법은 무엇입니까?
다른 혼합 방법에 대한 총 온도를 계산하는 방법은 무엇입니까?
가스의 단열 변동 하에서 엔트로피 합이 증가하는 이유를 어떻게 설명할 수 있습니까?
15. 화학열역학의 기초
이기종 시스템은 해당 구성 요소의 창고가 특징입니다. 노래하는 마음의 경우, 이 창고는 시스템에 도입된 화학적 및 물리적-화학적 변형의 변동에 따라 변경될 수 있으며, 이로 인해 이전 것이 파괴되고 원자 사이에 새로운 결합이 형성됩니다. 이러한 과정은 이러한 결합의 두 가지 힘의 여파로 기 병합 에너지의 비전을 동반합니다.
화학 열역학은 열역학의 첫 번째 및 다른 속이 화학적 및 물리적 및 화학적 현상으로 발전하는 것을 살펴봅니다.
15.1. 화학 반응
화학 연설- 화학 창고, tobto의 거시적 몸체. tіlo, schodo 그런 것은 그러한 비율로 추가되는 화학 원소뿐만 아니라 ( 개별 화학 연설); 스미시또는 로친).
화학 연설 (선반)은 그것이 형성되는 요소와 її 채택을 위해 이러한 요소의 원자가 형성되는 것을 보여주는 화학식이 특징입니다.
새로운 연설의 확립으로 이어지는 okremy 화학적 연설 사이의 상호 관계 과정을 호출합니다. 화학 반응.
화학 반응이기 때문에 정방향과 역방향 모두에서 볼 수 있습니다.
닫힌 시스템에서는 시스템에 존재하는 피부 화학 요소의 양이 변하지 않는 방식으로 화학 반응이 관찰됩니다. 화학 반응이 참여하는 이유는 연설이 충분하지 않지만 화학양론적 양, 그 다음에. kіlkostі, scho vіdpovіdat 화학식 연설. 따라서 화학 반응은 음성 반응의 화학식과 반응 생성물의 화학식 사이의 등식으로 기록됩니다. 어서 해봐요 하지만 1 , 하지만 2 , …, 하지만 N- 출력 연설, 그리고 에 1 , 에 2 , …, 에 중- 반응의 Kіntsev 제품. 연설 사이의 동일한 화학 반응 하지만 1 , 하지만 2 , …, 하지만 N, 누가 연설의 끝을 불렀다 에 1 , 에 2 , …, 에 중, 평정심에 가입하십시오.
야코무에서 α 1 , α 2 , … α N, β 1 , β 2 … β 중- 화학양론적 계수. 예를 들어, 메탄 연소의 결과로 이산화탄소와 물이 용해됩니다.
CH 4 + 2O 2 \u003d CO 2 + 2H2O.
화학에서 단일 양의 연설에 대해 1이 허용됩니다. 마일 이 수량에는 Avogadro보다 오래된이 연설의 특정 수의 분자 (원자)가 있습니다. N ㅏ= 6.02204∙10 23 . 즉, 1몰의 말은 그러한 말의 양으로 간주되며, 그램 단위의 질량은 M의 가장 비싼 분자(원자) 질량입니다.
폴딩 시스템 창고 N 나두더지, 화학이 묻는다 어금니 부분시스템 구성 요소.
1. V=const에서 가스 혼합. 따라서 변화 이전과 이후에 가스를 차지하는 총 부피는 변화가 될 때까지 일정하고 가스로 채워져 부피 V 1, V 2, ... .. V n m 3 바이스 p 1, p 2, p n і 온도 T 1 T n , 그리고 이들 가스의 열용량 변화 s r / s v 더하다 k 1 , k 2 ,… 케이앤
온도
바이스
 (5.15)
(5.15)
몰 열용량이 같고 k 값이 같은 가스의 경우 공식 (62) 및 (63)은 다음과 같습니다.
2. 가스 흐름의 변화. 변동하는 vitrati 스트림의 수는 M 1, M 2, ... M n, kg / year, vitrati의 부피 - V 1, V 2, ..... V n m 3 / year, 바이스 가스 - р 1 , р 2 , р n і 온도 - Т 1, Т 2, ... Т n, 그리고 다른 가스의 청색 열용량이 같으면 k 1, k 2, .... k n 다음 총 온도는 다음 공식에 의해 결정됩니다.
 (5.18)
(5.18)
T의 온도와 그 반대의 온도에서 1시간 동안 vitrata 합계의 부피:
 (5.19)
(5.19)
가스의 경우 k 값이 같다면 합산 온도는 공식 (64)에 의해 결정됩니다. k 값이 같은 가스 흐름에 문제가 있는 경우 공식 (66)과 (67)은 다음과 같습니다.
 (5.21)
(5.21)
관리자
5.1. 첫 번째 cob mill t 1 \u003d 300 0 С에서 t 2 \u003d 50 0 С에서 마지막 것으로 전환하는 동안 1kg의 내부 에너지 변화를 다시 알기 위해. kJ 단위로 날짜를 알려주십시오.
내부 에너지의 변화는 공식(5.9)으로 알려져 있습니다.
Du \u003d W vm (t 2 -t 1).
Koristuyuchis 탭. 4.3, 검토에 필요
(Z vm) 0t =0.7084+0.00009349t kJ/(kg·K);
(3 vm) 50300 = 0.7084 +0.00009349 (50 +300) = 0.7411 kJ / (kg·K).
외체,
Du = 0.7411(50-300) = - 185.3kJ/kg
Vidpovid: DU = - 185.3 kJ/kg
5.2. 내부 에너지 2m 3의 변화를 다시 알면 온도가 t 1 \u003d 250 0 С에서 t 2 \u003d 70 0 С로 감소합니다. 다시 코브 바이스 P1 = 0.6 MPa.
Vidpovid: DU = -1063kJ.
5.3. ruhomy 피스톤으로 실린더에 넣은 가스에 100kJ의 열이 호출됩니다. tsimu에서 vikonan 작업의 값은 115 kJ가 됩니다. 가스의 내부 에너지를 크게 변경하여 비용이 0.8kg입니다.
Vidpovid: DU = - 18.2kJ.
5.4. 압력 0.5MPa, 온도 50℃에서 2m 3회를 압력 0.2MPa, 온도 100℃에서 10m 3회 반복에서 변경한다. 압력과 전체 온도를 설정한다.
Vidpovid: t cm = 820С; Рcm = 0.25MPa.
5.5. 보일러 실의 선택된 가스 연도에서 3 개의 보일러의 가스가 펄럭이며 어느 것이 가고 어느 것이 대기압을 누릅니다. 단순화를 위해 동일한 가스가 동일한 창고를 가질 수 있음을 인정합니다. CO 2 = 11.8%; O2 = 6.8%; N2 = 75.6%; H2O = 5.8%. Vartov vitrati gazіv는 V 1 \u003d 7100 m 3 / 년을 설정합니다. V 2 \u003d 2600m3 / 년; V 3 \u003d 11200 m 3 / 년, 가스 온도 환기 t 1 \u003d 170 0 С, t 2 \u003d 220 0 С, t 3 \u003d 120 0 С 온도.
Vidpod: t = 147 0; V \u003d 20,900m 3 / 년.
5.6. 0.1MPa 압력의 3개 증기 보일러에서 나온 가스는 선택한 가스 덕트에서 이동하고 연기 파이프를 통해 대기로 방출됩니다. 가스의 체적 창고, 다음 공격 보일러에서 무엇을 해야할지 :
CO 2 = 10.4%; 찬성 2 = 7.2%; N2 = 77.0%; H2O=5.4%;
다른 사람에게서
CO 2 = 11.8%; O2 = 6.9%; N2 = 75.6%; H2O = 5.8%;
제삼
CO2 = 12.0%; O2 = 4.1%; N2 = 77.8%; H2O = 6.1%.
Vartovі vitrati gazіv 접기
M 1 \u003d 12000kg / 년; M 2 \u003d 6500kg / 년; M 3 \u003d 8400kg / 년; 가스 온도는 일반적으로 t1 = 1300C입니다. 티 2 \u003d 1800C; 티 3 \u003d 2000С.
선택한 가스 덕트를 변경한 후 가스의 온도를 결정합니다. 이들 기체의 몰 열용량이 같다는 것을 인정하십시오.
Vidpovid : t 2 \u003d 164 0 Z.
5.7. 가스 덕트에는 0.2MPa의 동일한 압력을 생성하는 세 개의 가스 흐름이 있습니다. 첫 번째 흐름은 200 0 C의 온도에서 vitrata V 1 = 8200 m 3 / year의 부피를 가진 질소이고, 다른 흐름은 500 0 C의 온도에서 7600 m 3 / year의 vitrata를 가진 이산화탄소이고 세 번째 포트는 세 번째 포트입니다. - 800 0 С의 온도에서 vitrata 6400 m 3 / year로 반복합니다.
Vidpod: t 1 = 423 0; V=23000 m3/년.
5.8. 최대 500 0 С까지의 냉각으로 인해 900 0 С의 온도에서 연간 400 kg의 증기 보일러의 가스 덕트에서 연소 생성물이 건조 설비로 바로 이동합니다. 가스는 20 °C의 온도에서 다시 가스 흐름과 흐름을 혼합하여 냉각됩니다. 두 가스 흐름의 압력은 동일합니다. R 가스 = R rev로 알려져 있기 때문에 매번 vitrata 연도를 계산합니다. 연소 생성물의 열용량은 고르게 취해야 합니다.
제안: M 턴. = 366kg/년.
동일한 압력으로 몇 개의 온도 조절 용기에 넣어 두십시오. 피 가지 하지만і 에에몰의 양으로 섭취. 이러한 선박을 적재할 때 전체 시스템에 따라 균일한 가스 저장소가 설치될 때까지 가스의 모방 변화가 있을 것입니다. 가스의 출력과 그 합이 이상 기체와 같다고 가정해 봅시다. 영구 가스 압력의 보존을 위한 Todi 피 합계에서 가스의 분압, 정착해야 할 것은 동일합니다.
낮 동안의 열 효과에서 이상 기체를 변경할 때 기체와 온도 조절 장치 간의 열 교환이 제어되지 않으며 시스템의 엔트로피 변화는 시스템 중간에서 프로세스의 비가역성을 의미할 가능성이 더 큽니다.
엔트로피의 변화를 알기 위해서는 설명된 모방 프로세스를 시스템의 동일한 코브와 엔드밀 사이의 명확한 전환과 비교할 필요가 있습니다.
가스의 똑같이 중요한 변화의 경우 케모 스탯이라고하는 온도 조절 장치와 유사하게 특수 가상 부착물에 의해 속도가 빨라집니다. . 이 부착물은 피스톤에 의해 문지르지 않고 움직이는 온도 조절 실린더에서 접혀 있습니다. 실린더 바닥에는 이 개별적인 화학적 음성을 위해 진동하면서 관통하는 막이 있습니다. 다른 선박에서 발견되는 뒤틀린 연설의 요약에서 개별 연설의 화장, chemostat의 zavantazhene에 남아 있습니다. На відміну від термостата, призначеного для підтримки заданої температури зануреного в нього тіла, або для нагрівання або охолодження останнього в рівноважному режимі, за допомогою хемостату забезпечують підтримання певного значення хімічного потенціалу даної індивідуальної речовини досліджуваної суміші речовин, а також рівноважне підведення та відведення речовини з суміші . 화학적 잠재력 나 - chemostat의 hochemical 구성 요소는 온도에 의해 명확하게 표시됩니다. 티바이스로 피스톤을 만듭니다. 피스톤의 압력을 변경하면 선택적 멤브레인을 통해 이 구성 요소의 전환을 직접 변경할 수 있습니다. 구성 요소의 화학적 포텐셜이 마지막 합계에 있으면 음성이 합계에 추가될 때 chemostat이 혼합되었을 때 합계에서 표시됩니다. Kvazirivnovaga는 멤브레인 측면을 따라 화학 포텐셜 값의 작은 차이로 멤브레인을 통한 연설의 확산 전이의 경우 합계의 합을 변경합니다.
이상 기체의 화학적 포텐셜은 가스가 개별 스테이션에서 알려져 있는지 또는 다른 이상 기체와 혼합되어 있는지 여부에 관계없이 간단히 다음과 같이 차이로 표현됩니다. 피 나є 또는 순수한 가스의 압력, 또는 합계의 분압. 따라서 이상 기체가 멤브레인을 통과할 때 합과 케모스타트 사이를 균등하게 투과하게 되며, 케모스탯에서의 압력과 합에서의 기체의 분압이 같은 것을 특징으로 한다.

쌀. 2.3. 마찬가지로 중요한 것은 추가 화학 조절 장치를 위한 두 가지 가스의 혼합입니다. ㅏ- 옥수수 밀 시스템; 비- 가스의 등온 팽창을 위한 밀 시스템; 안에- 멤브레인을 통해 zmіshuvannya gazіv 후 Kіntsevy 스탠; 1 – 개별 가스의 케모스탯 A와 B ; 2 – napіvproniknі 막; 3 - 동등하게 중요한 기체 혼합을 위한 용기.
마찬가지로 중요한 것은 이상적인 기체의 혼합입니다. ㅏі 비 2개의 케모스탯과 개별 구성 요소로 구성된 자동 온도 조절 시스템에서 수행 ㅏі 비, 세 번째 용기-우리가 정착 한 합계의 합계는 chemostat처럼 럼블 피스톤으로 고정합니다 (그림 2.3).
구성 요소의 두더지 형태로 chemostats의 cob 모멘트를 제거하십시오. ㅏ그 두더지 성분 비같은 바이스 아래 피
; sumishi를 선택할 때 피스톤이 0 위치에 있습니다(피스톤 아래의 가스가 0에 도달함). 혼합 과정은 두 단계로 수행됩니다. 첫 번째 단계에서는 가스의 등온 팽창을 변경해야 합니다. ㅏі 비; 누를 때 ㅏ보기를 줄이십시오 피
미리 정해진 악덕과 악덕까지 비 vіdpovіdno vіd 피
전에. Obsyagi, scho zamayutsya 가스는 첫 번째 및 다른 chemostats에서 vіdpovіdno vіd를 і іd로 변경합니다. 첫 번째 케모스타트에서 확장되는 가스에 의해 사악해진 로봇은 더 비쌉니다. ![]() ; 다른 사람에게
; 다른 사람에게 ![]() . 따라서 가상 부속서의 첫 번째 단계에서 전체 작업이 수행됩니다. 동일한 내부 에너지의 이상 기체의 등온 팽창을 가진 파편은 변하지 않습니다. Zvіdsi 협상 가능한 시스템의 엔트로피 변화는 동일합니다.
. 따라서 가상 부속서의 첫 번째 단계에서 전체 작업이 수행됩니다. 동일한 내부 에너지의 이상 기체의 등온 팽창을 가진 파편은 변하지 않습니다. Zvіdsi 협상 가능한 시스템의 엔트로피 변화는 동일합니다.
공정의 다른 단계(공기 혼합)에서 케모스타트의 가스는 선택적 멤브레인을 통해 흐름에 의해 동기화된 3개의 피스톤 요약으로 엄격하게 전달됩니다. 동시에 스킨 피스톤과 화학 조절기 및 컬렉션에 일정한 압력이 가해져 멤브레인을 통한 가스의 동일한 통과를 보장합니다(보다 정확하게는 컬렉션의 압력이 적습니다. 피 , 막을 통한 파괴적인 확산력에 대한 0의 영향 절약). 이 경우 변경 프로세스의 반대는 세 개의 피스톤 모두의 회전을 직접 동기식으로 변경할 수 있으므로 개별 구성 요소에 많은 혼란이 발생할 수 있습니다. 작업 완료 후 볼륨 컬렉션에서 대출을 분명히 합산하십시오.
다른 이상 기체의 조각은 열 효과, 낮 동안 다른 작업 단계에서 온도 조절 장치와 별관의 열 교환에 의해 영향을 받지 않습니다. Otzhe, 시스템의 엔트로피를 변경하는 것은 불가능합니다.
Corisno는 직접 pіdrahunk의 경로를 건너고 다른 단계의 가스 로봇은 0에 도달합니다. 케모스타트의 피스톤을 움직이기 위해 로봇을 사용하고 있으며 동시에 같은 크기의 로봇에 의해 수집기에서 가스가 운반되는 것이 사실입니다. Zvіdsi.
또한 변동하는 기체의 경우 엔트로피의 총 증가량은 viraz(2.9), . 똑같이 중요한 변화의 변형에도 불구하고 따뜻함의 회복과 등가 작업량의 가변성으로 인한 동점 수의 증가 ![]() , 그런 다음 가스의 직접적인(비가역적) 이동으로 엔트로피의 동일한 증가가 시스템 중간의 생성 흐름에 의해 구동됩니다. 강탈하지 않는 로봇 시스템이 없습니다.
, 그런 다음 가스의 직접적인(비가역적) 이동으로 엔트로피의 동일한 증가가 시스템 중간의 생성 흐름에 의해 구동됩니다. 강탈하지 않는 로봇 시스템이 없습니다.
대체(2.8) 및 viraz(2.9) 후 다음과 같이 다시 작성할 수 있습니다.
 . (2.10)
. (2.10)
역설의 요가를 통해 열역학 과정에서 spіvvіdnoshenyu vіdvoditsya obov'yazkové mіstse에. 엔트로피의 변화 (이상 기체를 바꿀 때!) 는 중요하지 않으며, 그러한 압력과 온도에서 변화합니다. 실제로 비공식 visnovok(2.10)이 여기에 소개됩니다.
yogo 갈색 비문이 있는 visnovok(2.10)을 추가했습니다. 구성 요소의 어금니 부분 소개 ![]() 그리고 viraz를 사용하여 엔트로피를 1 몰 합계에 대한 rozrahunka로 변경합니다.
그리고 viraz를 사용하여 엔트로피를 1 몰 합계에 대한 rozrahunka로 변경합니다.
![]() . (2.11)
. (2.11)
함수의 최대값은 기체의 등몰 합인 0.5에 따라 달라집니다.
이론의 관점에서 볼 때, 연설을 요약하면 구성 요소의 많은 몰수를 추가하면서 엔트로피 진동을 변경하기 쉽습니다. 비최대 하나의 축복 요소 ㅏ. (2.10) i 를 고려하면
(2.12)가 표시되었을 때 로그 함수의 수학적 표현은
 .
.
공식(2.12)은 합계의 마지막 확장이 집 구성 요소의 몰당 확장 엔트로피의 무한한 증가를 수반함을 보여줍니다.
공식(2.10)은 가스의 최종 양을 변경할 때 엔트로피 증가의 적분 값을 제공합니다. 콤팩트한 미분 솔루션에 도달하기 위해 열 전달에 대한 공식(2.7)과 유사하게 성분 혼합 모델(div. 그림 2.4)이 수정됩니다. 혼합물은 두 구성 요소가 모두 통과할 수 있는 멤브레인을 통해 도입되거나 심사위원을 분리하는 좁은 밸브를 통해 합계로 채워지는 것이 허용됩니다. ㅏі 비창고. 이 시스템은 온도 조절식으로 제어되며 두 용기 모두 보조 피스톤 뒤에 일정한 압력이 있습니다. 피 . 스웨덴어를 교환하는 경우 법원의 피부에 스미시를 보관하는 것은 동일한 명령의 법원에서 가져올 수 있습니다. 따라서 주어진 시스템은 전도성이 약한 칸막이가 있는 열교환 시스템과 유사합니다.
웃자 N 화학적으로 비대화형 그들 중에서 이상적인 가스 계속해서 열역학적 매개변수의 도움으로 변화와 마음이 바뀔 때까지 모든 구성 요소가 될 것입니다(필요한 매체와 결합된 마음). 알 필요가있다 똑같이 중요하다 매개변수는 변경 후 가스가 됩니다.
간단하게 변경하는 두 가지 방법을 살펴 보겠습니다. 프로세스가 무엇인지 고려해 봅시다. 필요한 매질과의 열교환 없이 .
2.1. Zmіshuvannya에서 W=상수
이런 기분으로 정신이 혼미해지도록 마음을 씻는다. 승 cob sum의 총합을 참조하십시오. 승희:
(길 잃은 흔적이 아니라 W H i부분적 의무 위, 단락 1.4.3에서 논의됨.)
크게:
P H i- 콥 바이스 나- 가스;
T H i,티 하이- 포차트코바 온도 나-th 가스는 0까지 적합합니다. 전에또는 0 지.
왜냐하면 전체 시스템 N마음에 zmіshuvanni가있는 가스 W=상수 zdіysnyuє zvnіshnії ї raboty가 아닌 경우 첫 번째 물결 ()에 대한 열역학의 첫 번째 옥수수 속으로 쓸 수 있습니다.
여기: 유 cm - 내부 에너지 summish 가스 질량 중 cm kg
온도 T 0K;
유 하이- 내부 에너지 나기체 질량 내가킬로그램
새싹 온도 T H i .
표기법을 소개하겠습니다.
유 cm - 정상 온도에서 가스 합계의 내부 에너지 공급 T 0K;
유 히 -애완 동물 내부 에너지 나-cob 온도가 있는 가스 T H i .
Todi 이퀄라이제이션(2.1.1)은 다음과 같습니다.
(2.1.2)
보시다시피 이상기체의 경우 뒤=C v dT vіdlіku vіdlіku vіdlіshnyої ї vіd에서 zvіdki 0 0 전에당신은 쓸 수 있습니다:
여기: - 범위의 평균 0 T 0K합계 가스의 질량 등방성 열용량;
범위에서 평균 0 T H i 0K질량 등방성 열용량 나가스.
대체(2.1.3)(2.1.2) 후 다음을 수행합니다.
그러나 단락 1.4.10까지 전체 가스의 질량 열용량은 구성 요소의 질량 분율을 통해 표현됩니다. 미군 병사다음 순서로 정확한 열 용량:
범위 내 평균과 유사 0 T 0K가스 합계의 질량 등방 열용량은 다음과 같이 지정됩니다.
방정식(2.1.4)의 왼쪽 부분에 이 바이러스를 대입하면 다음과 같습니다.
별 (2.1.5)
왜냐하면 나는 평등해질 것이고, 그 다음 대체 후에 내가같을 때까지 (2.1.5) 우리는 여전히 합계 온도에 대한 공식을 취합니다. N가스:
보시다시피 공식(2.1.6)은 공격적인 방식으로 작성할 수 있습니다.
(다음에 tvir이 0~ T H i 0K어금니 등온 열용량 나일 가스.)
고급 문헌에서 온도에서의 열용량의 경험적 축적은 종종 다음 범위에 대해 제공됩니다. 0 티 0 С .
대입(2.1.8)과 (2.1.9)가 같을 때까지(2.1.2) 다음을 수행합니다.
교체 내가이 값의 경우 총 가스 온도(도) 공식 섭씨 :
비슬로블류치 나는분자량을 통해 공식을 하나 더 뺍니다.
공식 (2.1.6), (2.1.7), (2.1.10) 및 (2.1.11)의 부호에서 평균 열용량이 측정되며, 상한선은 총 온도로 평균화됩니다 ( 티또는 티), 약속의 목적은 무엇입니까? 이 때문에 총 온도는 다음 공식에 의해 결정됩니다. 마지막 접근 방법 .
2.1.1. 가스 변동의 개인 변동 W=상수
수식 (2.1.6), (2.1.7), (2.1.10) 및 (2.1.11)의 몇 가지 예를 살펴보겠습니다.
1. ghazis가 포효하도록 하지 마십시오. 나까지온도를 변경할 수 있습니다.
(진짜 전에온도 증가에 따른 변화, 즉 최대.
드 쓰레기 , ㅏ- 경험적으로 긍정적인 계수.
0에서 2000 0 C 범위의 기술 rozrahunkiv의 경우 다음 공식으로 계산할 수 있습니다.
a) 이원자 기체의 경우 전에 1,40 - 0,50 10 -4 티;
b) 연소 생성물 전에 1,35 - 0,55 10 -4 티.
공식 목록에서 adiabati 디스플레이에 온도를 주입한 것을 볼 수 있습니다. 전에섭씨 온도보다 수백도 낮은 온도에서는 눈에 잘 띄지 않습니다.
그래서, 약초 렛고, 쇼
그런 다음 공격적인 모습에 대한 공식(2.1.6):
공식 (2.1.12)는 공식 (2.1.6), (2.1.7), (2.1.10) 및 (2.1.11)에 대한 첫 번째 근사치로 승리할 수 있습니다.
2. 번개와 등각 열 용량이 동일하고 이러한 열 용량의 축적이 온도의 영향을 받을 수 있는 가스가 변동하도록 하십시오.
Todi 이퀄라이제이션(2.1.7)은 간단해 보입니다.
가스의 몰 열용량과 등온 열용량이 동일하므로 Mayer와 같을 가능성이 높습니다.
buti가 서로 같고 작은 isobarnі 열 용량과 adiabati, tobto의 동등한 표시로 인해.
생각해보면 같음(2.1.12)은 (2.1.13)으로 변환됩니다.
2.1.2. 가스 변동 후 Tisk W=상수
가스 변동 후 복원되는 압력은 단락 1.4.2의 공식 또는 마음에 의해 결정될 수 있습니다.
아르 자형센티미터 승센티미터 = 중센티미터 아르 자형센티미터 티= 중센티미터 티.
우리는 주유소의 세 개의 수평 볼 A, B 및 C를 명확하게 볼 수 있으며 확장 볼은 A보다 크고 A는 C보다 높습니다. 창고와 C에 두 가지 금액으로 퍼질 수 있습니다.
Tse zmіshuvannya 그 podіl dvoh gazіv는 zdіysniti і 턴어라운드 방식, zmіtsnivshi A, B 및 C 수평 트럼펫이 될 수 있습니다. 이름의 주유소에서 나오는 스킨 파이프의 끝은 피스톤으로 닫힙니다. 이제 볼 B와 C의 중간에 피스톤을 놓고 돌진하고 오른쪽으로 화를 내고 A 지점에서 피스톤을 오른쪽으로 부른 다음 오른쪽으로 부를 것입니다. . Todi B 및 C deyakі masi 가스 pіdut zі stovpa 및 A, navpaki, nadіyde yakіs obsyag sumіshi. 우리는 그러한 스킨 튜브에서 파이프가 생각 나게하는 가스 기둥의 수평 공인 동일한 창고의 덩어리의 덩어리가 있음을 인정합니다.
![]()
rivnyan에서 동일하게 할당되는 의미
다음을 참조하십시오
![]()
이제 늑대인간처럼 합을 나누어 얼룩진 로봇을 격려하자.
혼자 obyagu sumishi, z i vevemo, vіdpovіdno, obyagi에 소개되었습니다.
공정으로 얼룩진 전체 작업은 비용이 많이 듭니다.
이 값을 Bachimo로 대체하면 이 로봇은 0이 됩니다.
여기에 미묘함의 듀스가 있습니다. sumishi와 yaks에서 sumisha A는 떨어져서 높이와 pridbali의 높이에서 들어 올려졌습니다. 그러나 로봇이 0에 도달하고 시스템의 온도가 일정하면 시스템이 많은 열을 주거나 빼앗기 때문에 이 경우에는 덜할 수 있습니다. 위치 에너지의 변화를 알면 열의 양을 알 수 있고 시스템이 개선되며 별과 엔트로피의 변화를 알 수 있습니다.
창고의 위치 에너지 증가
그러나 엔트로피의 증가가 1이 되도록 시스템에 열을 추가하는 것이 더 비쌉니다.
이러한 엔트로피 총합과 총합 C의 합 값은 엔트로피 단위 총합 A보다 큽니다. 합 B와 C의 총합을 알 수 있으며, 이러한 엔트로피 단위 총합의 엔트로피 합은 ㅏ; 역등온 방식에 의해 총 합 B와 Z를 합으로 가져오는 것이 가능하며, 프로세스가 바이라아제(75)와 동일한 두 합의 엔트로피 증가는 역부호로 취합니다.
총 재고에 대한 엔트로피 증분
![]()
![]()
갭을 통한 견고함을 위한 이퀄라이제이션(76) viraz로 대표 가능